近日,中国科学院昆明动物研究所研究员刘振和昆明医科大学药学院暨云南省天然药物药理重点实验室副教授郑昌博团队,以“pleiotropy ofd positive selection in ancient ace2 suggests an alternative hypothesis for bat-specific adaptations to host coronaviruses”为题,在期刊proceedings of the national academy of sciences of the united states of america(pnas,美国国家科学院院刊, 综合性1区top期刊,if:9.58)发文,阐述发现蝙蝠的飞行功能演化与抗冠状病毒之间的协同演化关系。
中国科学院昆明动物研究所郭媛婷和蒋继滨以及昆明医科大学药学院暨云南省天然药物药理重点实验室乔冠荣为论文共同第一作者。中国科学院昆明动物研究所研究员刘振和昆明医科大学药学院暨云南省天然药物药理重点实验室副教授郑昌博为论文通讯作者。该研究工作得到了国家重点研发计划、国家自然科学基金、中国科学院相关项目的资助。
由于新冠肺炎的流行,血管紧张素转化酶2(ace2)已成为生物医学中最具治疗靶向的人类分子之一,因为ace2是sars-cov和sars-cov-2侵入细胞不可或缺的主要受体;同时,ace2在心脏中高表达,且其似乎是一种对心脏具有保护作用的分子。有学者研究发现感染sars-cov-2的患者,心血管疾病(cvd)的患病率较高,且>7%的患者因感染sars-cov-2而经历心肌损伤。
众所周知,蝙蝠作为唯一能真正飞行的哺乳动物,也是各种病毒的宿主。这些病毒会导致人类患上严重疾病,类似于亨德拉病毒、马尔堡病毒、埃博拉病毒以及新冠病毒。蝙蝠在漫长的进化中,出现了一系列与ace2功能密切相关的适应性表型:一方面,蝙蝠的心脏功能变强,心率调控能力增加。蝙蝠在飞行时,心率高达900bpm,但在静止休息时,心率最低可降至200bpm左右,这有助于减少能量消耗;另一方面,尽管携带多种可以造成多种人畜共患的病毒,但是蝙蝠自身很少或不会表现出相应的疾病症状。这些现象提示着,蝙蝠祖先的ace2可能经历了自然选择作用,影响了与蝙蝠飞行和抗冠状病毒相关的功能。
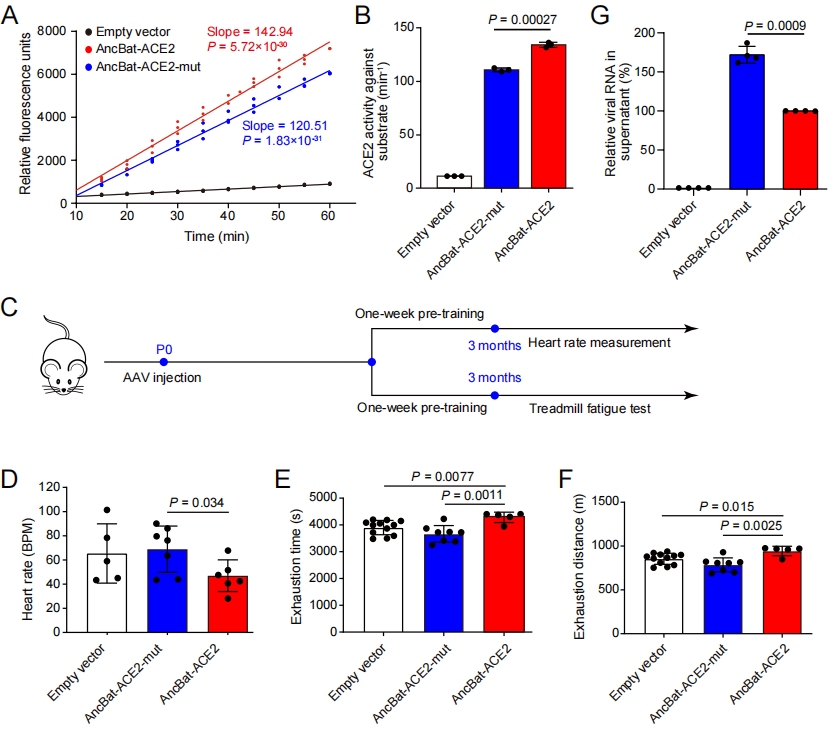
为了验证上述假说,刘振团队和郑昌博团队检测了蝙蝠祖先枝系上ace2的选择压力情况,结果发现蝙蝠祖先ace2(ancbat-ace2)确实存在显著的正选择信号,并且鉴定出了10个受到正选择的氨基酸位点。为了验证这些正选择位点的功能效应,研究团队通过重建蝙蝠祖先的ace2蛋白,以及改变祖先序列中的正选择位点的突变体(ancbat-ace2-mut)进行实验,结果发现,与突变体(ancbat-ace2-mut)相比,蝙蝠祖先ace2(ancbat-ace2)具有显著更强的酶活性。为了进一步验证ace2在蝙蝠祖先枝系上所受选择压力对心脏功能的影响,研究团队利用心脏特异表达的腺相关病毒(aav9)分别将ancbat-ace2和ancbat-ace2-mut转染至小鼠心脏中,并对这些小鼠进行跑步机疲劳测试。结果发现,携带ancbat-ace2的小鼠比携带ancbat-ace2-mut的小鼠的心率调节能力和运动能力都显著增强。进一步地,研究团队利用感染实验分别检测了ancbat-ace2和ancbat-ace2-mut与新冠病毒sars-cov-2的亲和性,结果发现,相较于ancbat-ace2-mut,ancbat-ace2与sars-cov-2的亲和力显著更低。这些结果表明,自然选择对蝙蝠祖先ace2两种功能造成了影响,提示着蝙蝠的飞行演化与抗冠状病毒之间的协同演化关系,该结果为蝙蝠如何进化出防御冠状病毒的机制提供了新的理解。



